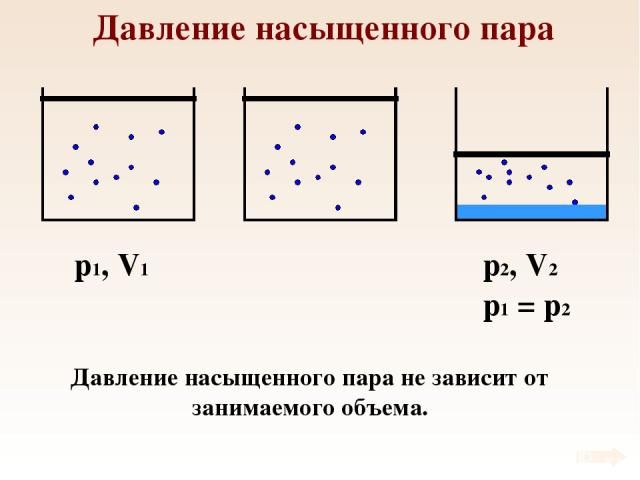
Почему давление насыщенного пара не зависит от объема
Почему давление насыщенного пара не зависит от объема
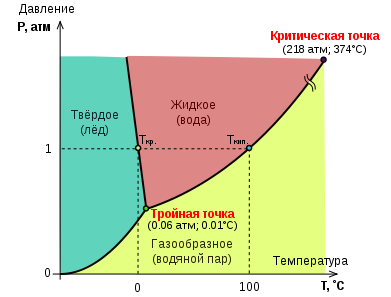
Давление насыщенного пара — это физическая характеристика вещества, которая описывает его склонность к переходу из жидкого или твердого состояния в парообразное. Одним из важных свойств насыщенного пара является тот факт, что его давление не зависит от объема. Почему так происходит? Объяснение этому феномену связано с термодинамическими процессами, происходящими в газах. Давление газа зависит от количества молекул, которые сталкиваются с поверхностью, на которую они действуют.
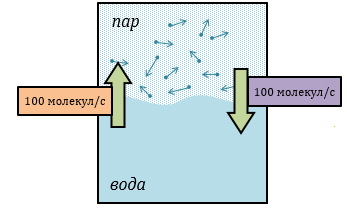
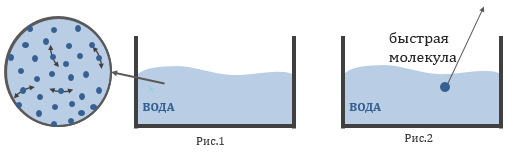
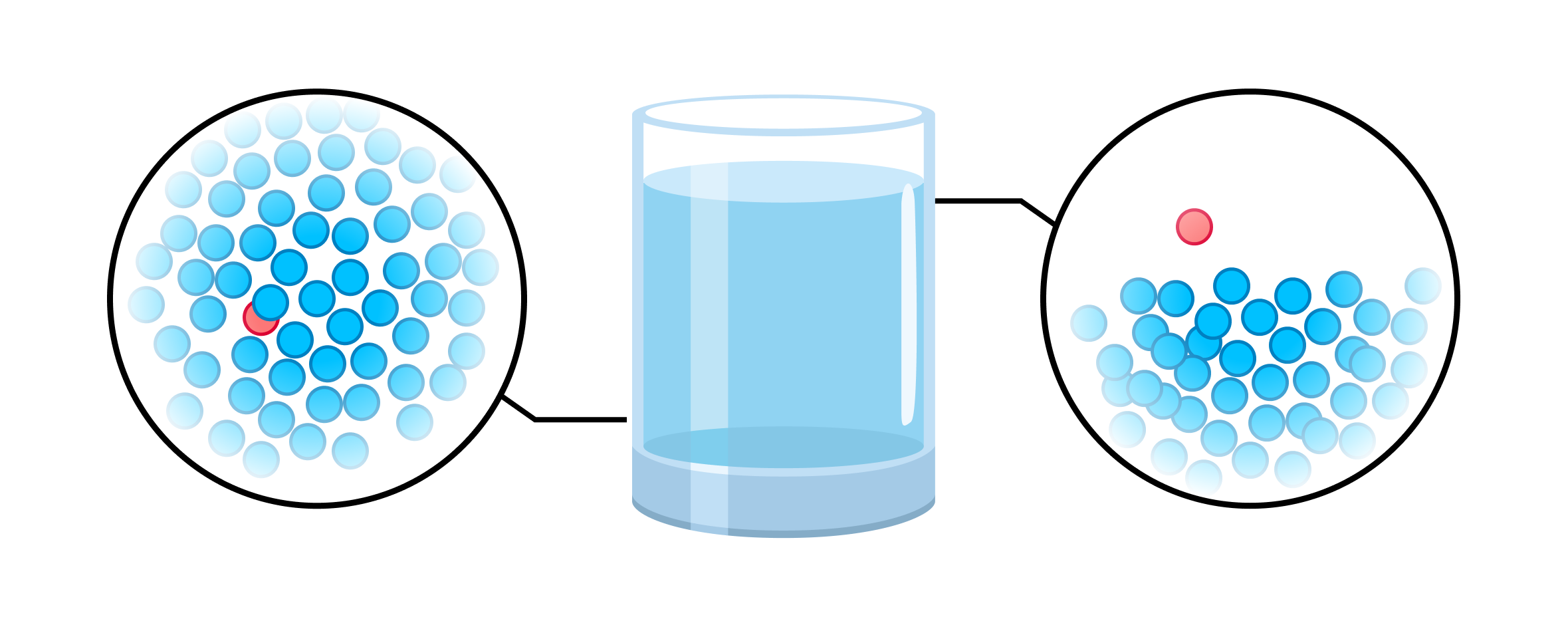



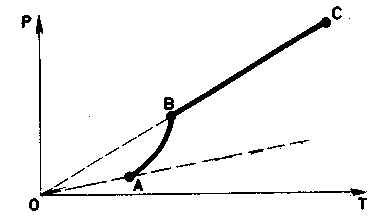


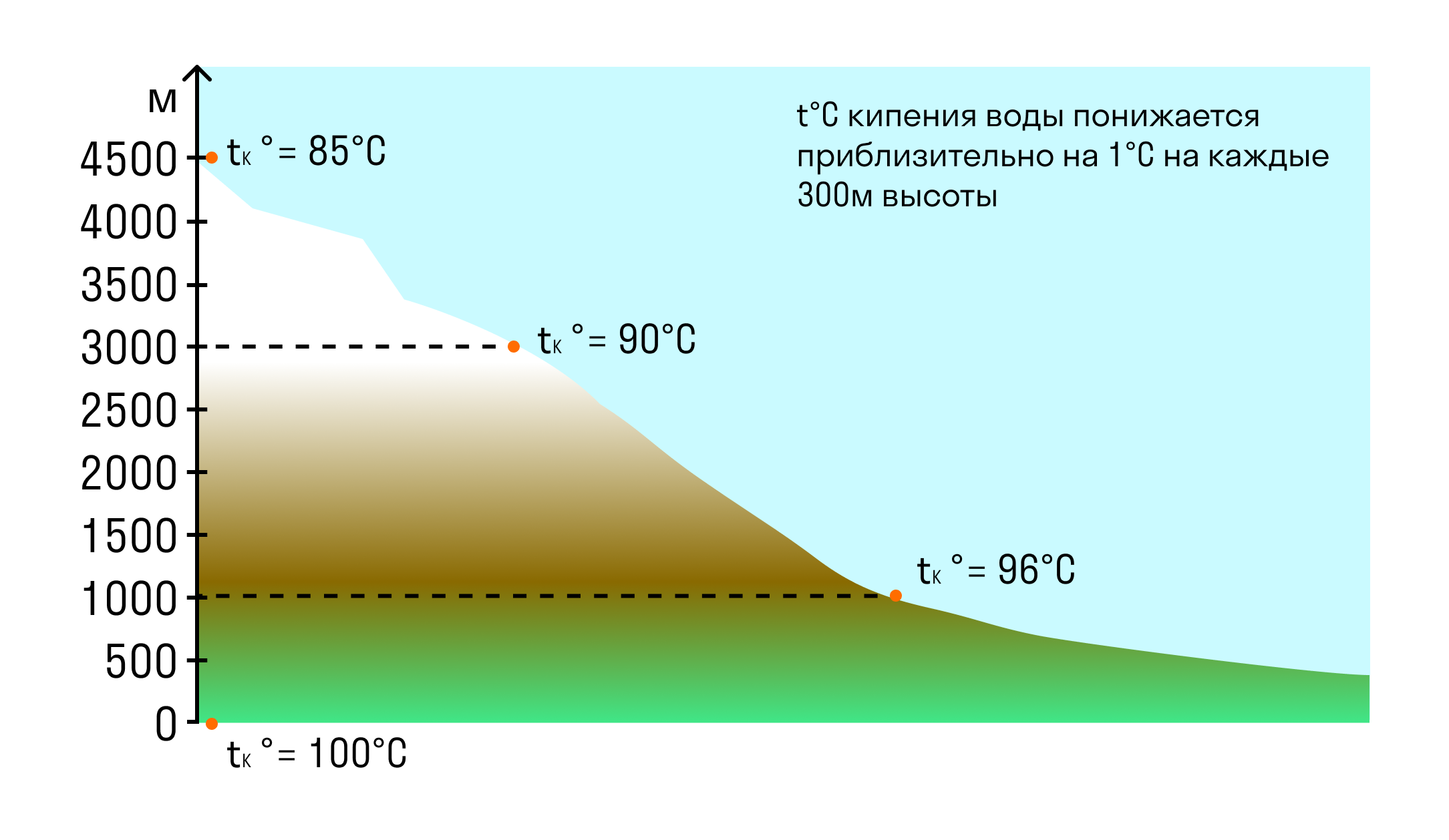
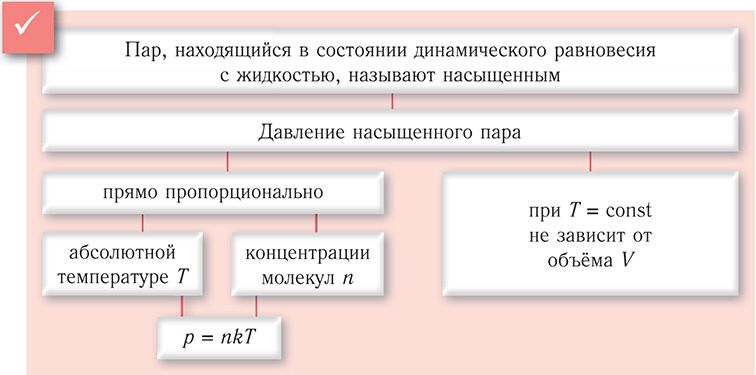
Насыщенный пар - это такой пар, который находится в динамическом равновесии со своей жидкостью. Количество молекул, покидающих жидкость в результате испарения, равно количеству молекул, возвращающихся в жидкость. Давление насыщенного пара зависит от температуры см. Давление насыщенного пара не зависит от объема пара. Формулы, где встречается характеристики насыщенного пара: Влажность воздуха.
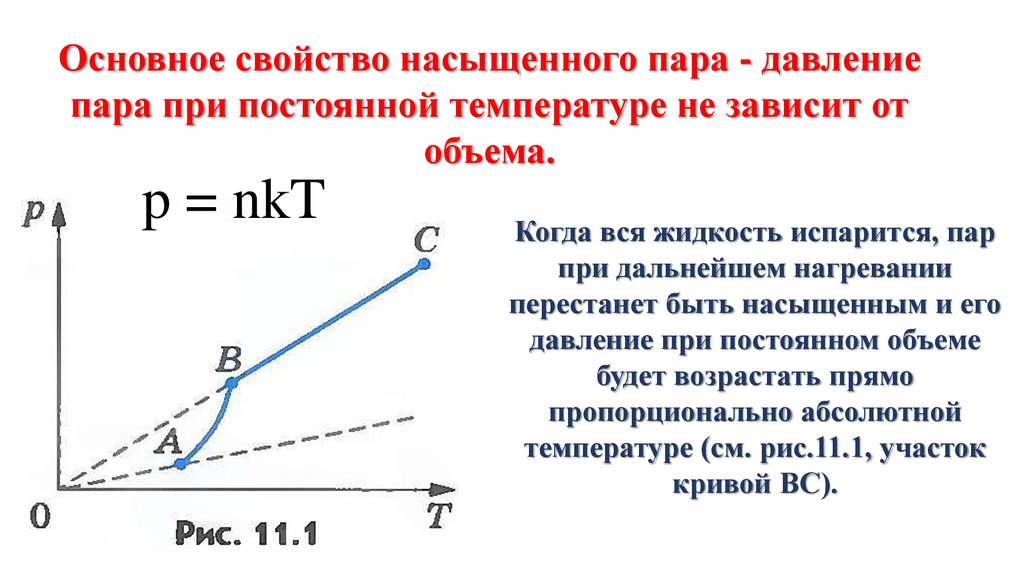


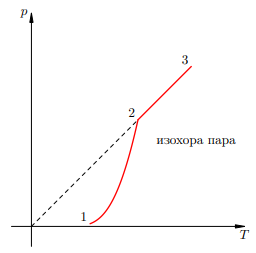

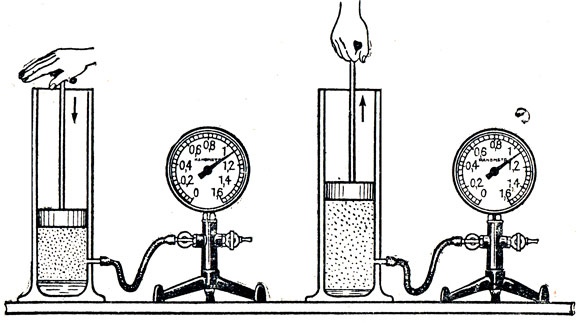
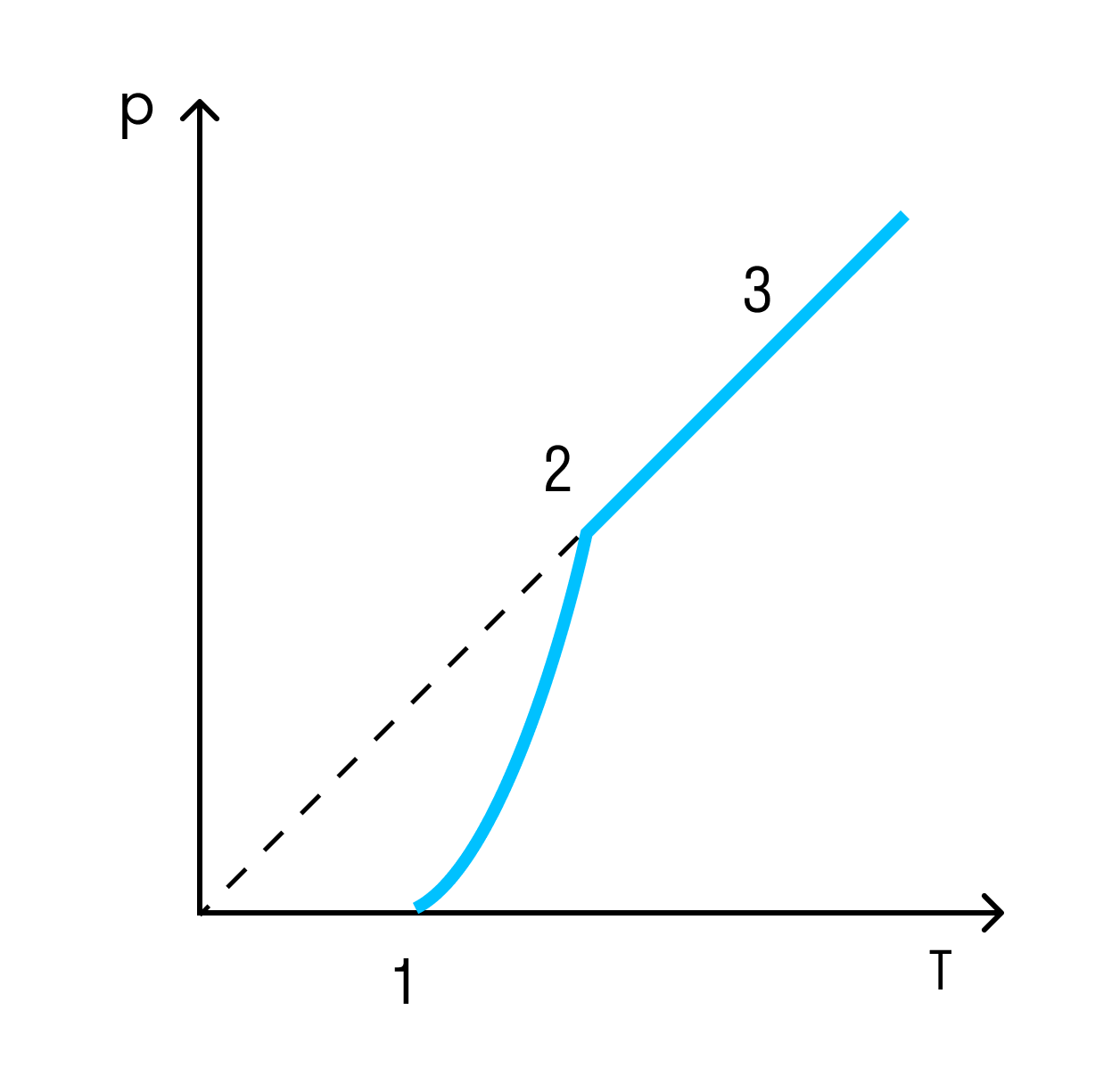
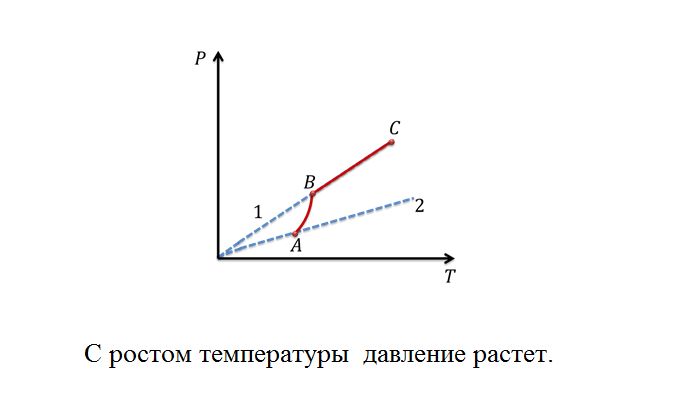
Поэтому давление насыщенного пара зависит от молекулярной структуры жидкости. Давление насыщенного пара жидкости, состоящей из сильно взаимодействующих друг с другом молекул, меньше, чем давление насыщенного пара жидкости, состоящей из слабо взаимодействующих молекул. С увеличением температуры давление насыщенного пара растет быстрее, чем идеального газа. При нагревании жидкости в закрытом сосуде давление пара растет не только из-за повышения температуры, но и из-за увеличения концентрации молекул массы пара вследствие испарения жидкости. С идеальным газом этого не происходит. Когда вся жидкость испарится, пар при дальнейшем нагревании перестанет быть насыщенным и его давление при постоянном объеме будет прямо пропорционально температуре.